它被誉为“重大”突破。
世界知名专家甚至大胆宣称lecanemab 改变游戏规则的结果代表了阻止阿尔茨海默氏症残酷进展的“终结的开始”。
可是什么药呢?它是如何工作的?
在这里,MailOnline 回答了您关于 lecanemab 的所有问题,包括何时可以将其提供给英国和美国的患者。

日本制药公司研制的药物卫材 (Eisai) 和美国生物技术公司百健 (Biogen) 共同创建,用于治疗大脑中淀粉样蛋白患者的轻度认知障碍
相关文章
上一页 1 下一页 布雷亚kthrough 阿尔茨海默氏症药物可能标志着“...的开始”
布雷亚kthrough 阿尔茨海默氏症药物可能标志着“...的开始” 记录从捐赠的精子中出生的婴儿数量:评分...
记录从捐赠的精子中出生的婴儿数量:评分...  救护人员进行第一次罢工30 年:999... ="mol-para-with-font">Lecanemab 每两周输注一次,给予阿尔茨海默病早期阶段的患者。
救护人员进行第一次罢工30 年:999... ="mol-para-with-font">Lecanemab 每两周输注一次,给予阿尔茨海默病早期阶段的患者。它被设计为对c了解淀粉样蛋白的积聚——大脑中的有毒斑块被认为会导致残忍的、夺取记忆的疾病。
伦敦大学学院世界领先的痴呆症研究人员和分子生物学家约翰·哈迪教授(如图)说,这种药物“代表着终结的开始” '
告诉免疫系统从大脑中清除淀粉样蛋白的抗体治疗是由 Japa 制造的日本和美国制药公司 Eisai 和 Biogen。
试验表明了什么?
lecanemab 的 III 期试验评估了该药物在 1,795 名早期阿尔茨海默氏症患者中减少认知和功能衰退的能力。
一半的参与者每两周服用 10mg/kg 的药物,而其他人则服用安慰剂。
研究人员在开始研究前和 18 个月后再次测量了所有参与者的记忆力、判断力、解决问题能力和判断力。
结果显示,接受 lecanemab 治疗的人的精神状况比接受假人治疗的人低 27%。
扫描显示,Lecanemab 接受者的大脑中淀粉样蛋白的积累速度也较慢。
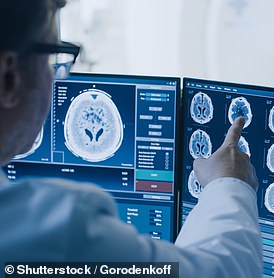
src="/uploads/allimg/221130/2119194048-8.jpg" height="398" width="634" alt=" Lecanemab 每两周一次输液给处于阿尔茨海默病早期阶段的患者(库存)” class="blkBorder img-share" style="max-width:100%" />Lecanemab 每两周一次输注给阿尔茨海默病早期阶段的患者(库存)
结果在旧金山的一次医学会议上公布,并发表在著名的新英格兰医学杂志上。
阿尔茨海默氏症药物的突破可能标志着几十年后的“终结的开始”-长期寻找治疗方法以阻止残酷的记忆衰退阿尔茨海默氏症在未来可能会通过尿检被发现药物危险吗?
专家警告说,突破性药物被标记为“痴呆症终结的开始”,对脑出血风险存在疑问
一些专家这么说吧,考虑到脑出血的风险,可能无法在 NHS 上安全地推出 lecanemab
Advertisement除了令人鼓舞的结果,该试验还提出了一些安全问题。
12.5% 的 lecanemab 组发现脑肿胀,而安慰剂组为 1.7%。
卫材和百健坚持认为,虽然它出现在扫描中,但其中许多病例没有症状。
数据还显示lecanemab 组有 17% 的人出现脑微出血,而安慰剂组为 8.7%。
制药业老板坚称这些数字在预期范围内。
在目前正在调查的事件中,还有两名患者在试验期间服用 lecanemab 时死亡。
然而,Eisai 和 Biogen 指出,所有可用的安全信息都表明该疗法与死亡风险增加无关。
距离推出还有多远?
制药商正在寻求 lecanemab 的批准美国食品和药物管理局,预计将于 1 月初做出决定。
这些公司表示,他们还将向日本和欧洲的监管机构提交他们的调查结果,以便2023 年 4 月。
但是,监管机构随后需要在做出决定之前评估药物是否安全有效。
专家认为该药最早将于 2023 年提供给英国患者。
怎么样与类似药物 Aduhelm 不同?
Aduhelm 和 lecanemab 均由Eisai 和 Biogen — 是旨在去除淀粉样蛋白沉积物的抗体。
然而,lecanemab 靶向尚未聚集在一起的淀粉样蛋白。
Aduhelm 去除大脑中形成的淀粉样斑块。
Aduhelm 的批准对阿尔茨海默病患者来说是一个罕见的亮点,但批评者警告说该药物的疗效不佳,并且强调了它的风险。
不是已经有治疗阿尔茨海默氏症的药物了吗?
目前没有可用的阿尔茨海默氏症治疗方法,数十年的试验一再未能产生成功的治疗方法。
然而,药物被用来对抗明显的症状。
近 100 万英国人和 700 万美国人患有痴呆症——其中多达四分之三的病例被认为是由阿尔茨海默病引起的。
澳洲中文论坛热点
- 悉尼部份城铁将封闭一年,华人区受影响!只能乘巴士(组图)
- 据《逐日电讯报》报导,从明年年中开始,因为从Bankstown和Sydenham的城铁将因Metro South West革新名目而
- 联邦政客们具有多少房产?
- 据本月早些时分报导,绿党副首领、参议员Mehreen Faruqi已获准在Port Macquarie联系其房产并建造三栋投资联